| |
Laure Schalchli dans mensuel 301
daté septembre 1997 -
Des millions d'anticorps et un grand principe : pour reconnaître l'étranger, encore faut-il se connaître soi-même
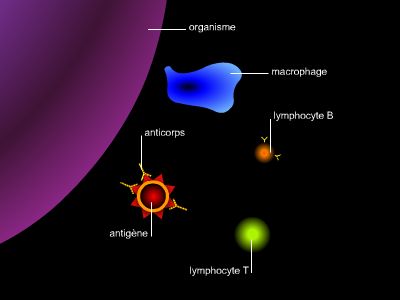
La masse du système immunitaire est comparable à celle du foie ou du cerveau. Mais il est éparpillé dans tout l'organisme. En font partie les globules blancs circulant dans le sang, dans la lymphe et imprégnant les tissus. Les principales cellules de l'immunité sont les lymphocytes, qui sont les globules blancs majoritaires dans le sang. Un homme adulte en contiendrait quelque deux mille milliards. Mais il existe beaucoup d'autres cellules impliquées dans l'immunité : globules blancs polynucléaires, monocytes ou macrophages, mastocytes, cellules dendritiques.
Le système immunitaire c'est aussi une série d'organes et de tissus dits lymphoïdes : les ganglions, la moelle des os, la rate, les amygdales, les végétations, l'appendice et des tissus associés au tube digestif et aux poumons en font partie. S'y ajoute le thymus, un organe situé dans le thorax derrière le sternum, qui grossit jusqu'à la puberté puis s'atrophie à l'âge adulte.
Toutes les cellules impliquées dans l'immunité prennent naissance dans la moelle des os. Certains lymphocytes se différencient dans le thymus. Puis ils migrent dans le sang et la lymphe et séjournent temporairement dans la rate, les ganglions, en se concentrant à proximité de la peau et des muqueuses, partout où le risque de pénétration d'intrus est grand. En permanence, le système immunitaire assure l'intégrité de l'organisme face aux substances étrangères, aux bactéries, aux virus, aux parasites.
Quand a-t-il été découvert ?
Le 14 mai 1796, un médecin de Berkeley, Edward Jenner, fait une expérience capitale. Il prend au mot une croyance populaire, selon laquelle une maladie de la vache cowpox , maintenant appelée vaccine peut rendre l'homme réfractaire à la variole. Il introduit du pus d'une femme atteinte de la maladie bovine dans le bras du jeune James Phipps, un enfant de 8 ans en parfaite santé. Six semaines plus tard, il injecte au garçon du pus d'un malade atteint de variole. James Phipps reste en bonne santé. La vaccination est née.
Un peu plus de quatre-vingts ans plus tard, Louis Pasteur fournit un début d'explication au succès de Jenner. En injectant à des poules de vieilles souches atténuées de bacilles du choléra, Pasteur et Emile Roux les protègent d'une infection ultérieure par le même microbe, mais pas par d'autres germes. Pasteur répète l'expérience, entre autres, avec des bacilles du charbon inactivés par la chaleur. On trouve ici les propriétés essentielles des réactions immunitaires : la vaccination ne protège que contre l'agent vaccinant spécificité, la protection est complète efficacité, le vaccin protège pendant des années, voire toute la vie mémoire.
Peu après, le zoologiste et microbiologiste russe Ilya Mechnikov propose sa théorie « cellulaire » de l'immunité, qui fait intervenir des cellules spécialisées. Pour la première fois, il suggère que l'inflammation n'est pas une composante nocive de la maladie, mais une réaction de l'organisme qui tend à protéger le malade. C'est au tournant du siècle que la réaction immunitaire est rattachée à l'apparition dans le sang de protéines spécifiques, les anticorps. En 1890, l'Allemand Emil von Berhing et le Japonais Shibasaburo Kitasato isolent les premiers d'entre eux, des substances solubles capables de neutraliser les toxines diphtérique et tétanique.
Qu'est-ce qu'un anticorps ? Comment est-il fabriqué ?
Le nom d'abord, anticorps, vient de ce que cette substance reconnaît le corps étranger et s'y fixe. On ne parle pas d'anticorps sans parler de son partenaire obligé, l'antigène, nommé ainsi parce que c'est justement... le « générateur » d'anticorps. L'antigène est le composé qui, quand on l'introduit dans l'organisme, provoque la formation d'anticorps spécifiques dirigés contre lui. La définition se mord la queue.
Les anticorps sont des protéines solubles présentes dans le sang. On les appelle également immunoglobulines. Elles sont fabriquées par un type particulier de globules blancs, les lymphocytes B. Le sang humain en contient une quantité énorme : un litre recèle environ soixante-dix grammes de protéines, dont dix à vingt grammes d'immunoglobulines.
Un casse-tête a dès le départ préoccupé les immunologistes. Un anticorps reconnaît de façon extrêmement fine et spécifique un antigène. Or il existe, dans la nature, un nombre indéfini d'antigènes. Le système immunitaire peut donc produire des anticorps contre n'importe quoi, y compris des substances créées par l'industrie chimique du XXe siècle.
Pour l'expliquer, on a d'abord pensé que les anticorps s'adaptent à l'antigène injecté, qu'ils « apprennent » sa forme en s'y modelant. Ce modèle, dit instructionniste, a été défendu jusqu'à la fin des années 1950. Il a été détrôné par celui de la « sélection » des anticorps : une diversité énorme d'anticorps existe bel et bien dans l'organisme. L'arrivée d'un antigène sélectionne ceux qui le reconnaissent et s'y fixent. Un processus somme toute très darwinien. Le modèle de la sélection supposait cependant de résoudre un problème de taille : la fabrication de millions d'anticorps différents, bien plus que le nombre total de gènes disponibles dans les chromosomes.
Deux phénomènes génétiques exceptionnels, qui ont lieu dans les lymphocytes, assurent une telle diversité. Ils ont été découverts pendant les années 1970. Le premier est un « remaniement » du génome. Chaque anticorps est codé par un gène unique, construit à partir de plusieurs pièces détachées : au moins trois tronçons génétiques différents, choisis parmi plus d'une centaine, sont coupés et placés bout à bout. De plus, l'assemblage des tronçons est assez imprécis. Ce jeu de combinaisons permet de produire une diversité considérable d'anticorps, libérés par autant de lymphocytes différents. Des chiffres ont été avancés, très divers eux aussi : un million, dix milliards...
Le second processus laisse encore les généticiens perplexes. Certaines portions des gènes codant les anticorps mutent à une vitesse impensable dans le reste du génome. Le taux de mutation peut y être jusqu'à dix millions de fois plus élevé. Ce mécanisme, qui entraîne une augmentation extrême de la diversité, touche les anticorps déjà sélectionnés par l'antigène. Il a lieu dans les lymphocytes activés, en réponse à l'antigène, et se solde par la production et la sélection d'anticorps encore plus « performants ».
Notons enfin que contrairement à une simplification abusive, chaque antigène est reconnu par de nombreux anticorps différents. Et vice versa : un même anticorps reconnaît plusieurs antigènes. Les immunologistes parlent de dégénerescence de la reconnaissance.
Pourquoi rejette-t-on les greffes ?
Parce que l'organe greffé contient des composants, plus exactement des protéines, qui n'existent pas dans le corps du receveur. Le système immunitaire détecte ces protéines étrangères et détruit les tissus qui les portent.
Ces protéines spéciales sont appelées « molécules d'histocompatibilité » du grec histos , tissu. Elles ont des propriétés étonnantes. Normalement, à l'intérieur d'une espèce, donc chez l'homme, les protéines varient peu d'une personne à l'autre, sauf anomalie génétique. Dans le cas des molécules d'histocompatibilité, pour une seule protéine - c'est-à-dire pour un seul gène - on peut trouver plus de cent versions différentes dans la population. Comme ces protéines sont de surcroît assez nombreuses quelques dizaines, deux individus pris au hasard ont très peu de chances de porter les mêmes. Les protéines d'histocompatibilité sont ainsi de très bons marqueurs du « soi » biologique. Dernière particularité, toutes les cellules de l'organisme exhibent ces protéines à leur surface. A quelques exceptions près : les spermatozoïdes en sont dépourvus ; les globules rouges aussi, ce qui facilite les transfusions...
Ces protéines sont codées par un groupe de gènes, le « complexe majeur d'histocompatibilité » CMH. Qui est effectivement fort complexe et très étudié par les immunologistes et les généticiens. Il contient au moins une cinquantaine de gènes différents, mais seulement certains dits de classe I et II interviennent dans la reconnaissance du soi. Chez l'homme, on appelle souvent ces protéines HLA human-leucocyte-associated antigens , parce qu'elles ont été découvertes par hasard sur les globules blancs les leucocytes. On les distingue par des lettres : HLA A, B, C, E, F, G, DP, DQ, DR... Deux vrais jumeaux ont exactement les mêmes HLA. Deux frères et soeurs ont moins d'une chance sur seize d'hériter d'un lot identique. Connaissant la répartition des différentes formes de HLA dans la population, on estime que cette probabilité tombe à un sur 40 000 pour deux personnes prises au hasard.
D'autres protéines jouent un rôle mineur dans le rejet des greffes. Elles sont très variées et la liste est loin d'être close. L'une d'entre elles, « HY », est présente uniquement chez les hommes, car elle est codée par un gène situé sur le chromosome Y. Résultat : une femme rejette le rein ou le coeur d'un homme, même s'ils ont les mêmes HLA.
Comment le système immunitaire détecte-t-il les intrus ?
Dans les années 1970 a été faite une découverte étonnante : le système immunitaire n'est pas capable d'identifier les composés étrangers tels quels. Il ne reconnaît le « non-soi » que s'il est associé aux marqueurs du « soi » : les antigènes ne sont vus que s'ils sont portés, présentés par les protéines d'histocompatibilité. Tout est affaire de coopération entre cellules.
Très schématiquement, la reconnaissance de la plupart des bactéries qui pénètrent dans l'organisme se déroule de la façon suivante. En permanence, des sentinelles abondantes dans la peau, les muqueuses et les ganglions, les cellules dendritiques et les macrophages, captent les intrus et les ingèrent. Les antigènes bactériens sont digérés, fragmentés, puis exhibés à la surface de ces cellules. Ils n'y sont jamais exposés seuls, mais nichés au sein des protéines d'histocompatibilité. C'est sous cette forme que le système immunitaire les reconnaît. La reconnaissance est assurée par les lymphocytes : tous portent à leur surface des molécules semblables aux anticorps, mais ancrées sur la cellule. Ceux qui fixent spécifiquement l'antigène intrus sont sélectionnés et se multiplient. Entrent d'abord en jeu les lymphocytes T, baptisés ainsi parce que leur maturation se fait dans le thymus, puis les lymphocytes B, qui produisent les anticorps.
Autre cas possible : l'organisme est envahi par des virus. C'est la cellule infectée qui présente directement aux lymphocytes des fragments du virus, lovés dans les protéines du soi.
Lorsqu'un antigène a été reconnu une première fois, le système immunitaire s'en souvient. La mémoire repose sur des cellules à durée de vie extrêmement longue : elles - ou leurs descendantes - restent dans la rate, dans les ganglions, pendant des mois ou des années, prêtes à se réveiller si l'antigène réapparaît. En revanche, la très grande majorité des lymphocytes ne vivent que quelques jours : après avoir été activés et s'être multipliés à très grande allure pendant la réponse immunitaire, ils meurent en masse, se suicidant en réponse à des signaux externes. On ignore complètement ce qui permet à certains d'échapper à l'hécatombe.
Comment les détruit-il ?
L'organismerépond généralement à l'invasion de bactéries ou de virus par de la fièvre, puis par une réaction inflammatoire : le lieu de l'infection devient rouge, douloureux, gonflé. Les tissus infectés libèrent des substances chimiques qui dilatent les vaisseaux, provoquent un afflux de sang, attirent les globules blancs. Ces derniers affluent et détruisent les bactéries ou les cellules infectées. Si l'on entre dans les détails de la réponse immunitaire, l'affaire se complique très vite. Entrent en jeu une panoplie de cellules qui communiquent soit par contact physique, soit en libérant dans leur voisinage des signaux chimiques.
Les anticorps neutralisent les bactéries ou leurs toxines en les agglutinant et en activant contre elles des enzymes sanguines, regroupées sous le nom de système du complément. Mais ce n'est que l'une des armes du système immunitaire. L'entrée de bactéries provoque un recrutement en cascade. Les lymphocytes T « auxiliaires » ou CD4 activent les lymphocytes B, qui se multiplient et sécrètent les anticorps. Un seul lymphocyte peut en produire plus de dix millions par heure. D'autres cellules, les polynucléaires et les macrophages, ingèrent et tuent les microbes. La lutte contre les virus ou contre certaines bactéries se développant à l'intérieur des cellules fait intervenir d'autres acteurs, les lymphocytes T tueurs ou CD8. Ces derniers reconnaissent directement les cellules infectées et les tuent en y déclenchant un programme interne de suicide.
D'où viennent les maladies auto-immunes ?
La question est loin d'être vraiment résolue. Dans ces maladies, le système immunitaire s'attaque aux propres éléments de l'organisme : les cellules du pancréas dans certains diabètes, la gaine des neurones dans la sclérose en plaques, les globules rouges dans certaines anémies... L'élément déclenchant reste assez mystérieux. Un point est sûr : nous produisons tous des anticorps et des lymphocytes dirigés vers les constituants du corps humain. Certains pensent même que c'est indispensable à l'équilibre du système immunitaire. Mais en temps normal, ces lymphocytes sont inactifs.
Très tôt, durant la vie embryonnaire, le système immunitaire apprend à devenir tolérant vis-à-vis de ses propres constituants. Dans le thymus de l'embryon, beaucoup de lymphocytes dirigés contre les constituants du corps sont éliminés. D'autres sont simplement « muselés », empêchés d'agir on parle d'anergie des lymphocytes. L'hypothèse actuelle est que pour entrer en jeu un lymphocyte a besoin de recevoir au moins deux signaux. D'une part, il lui faut reconnaître l'antigène, présenté par une cellule adéquate. D'autre part, il doit recevoir en même temps un signal délivré par la cellule présentatrice, par contact direct ou sous forme d'une substance soluble. Dans l'embryon, ce second signal ferait défaut, ce qui entraînerait la mort ou l'anergie de tous les lymphocytes reconnaissant les constituants du corps.
Cette « éducation » du système immunitaire se poursuit à l'âge adulte. L'organisme fabrique en permanence des lymphocytes dirigés contre ses propres constituants. C'est la présence ou l'absence du second signal - qui reflète peut-être le danger associé à l'antigène - qui aiguillerait le système vers la tolérance ou vers la réaction immunitaire. Certaines maladies auto-immunes ont été associées à des HLA particuliers. La présentation de l'antigène par telle ou telle molécule d'histocompatibilité pourrait favoriser l'activation des lymphocytes dirigés contre les constituants du corps. Une autre piste est qu'une infection virale peut modifier la présentation des antigènes du soi et induire certains lymphocytes à y réagir.
Pourquoi un corps étranger comme le foetus est-il toléré par la mère ?
C'est ce qu'on appelle le « privilège immunitaire », qui profite d'ailleurs aussi aux cellules cancéreuses. Il n'existe pas d'explication unique à ce phénomène.
Pour le foetus, le scénario suivant est avancé. Lorsque l'oeuf se niche dans l'utérus, ses enveloppes ne portent pas les protéines d'histocompatibilité HLA classiques ; il échappe ainsi au rejet de greffe. Cependant, les cellules sans HLA sont normalement détruites par une catégorie spéciale de cellules immunitaires, les cellules tueuses naturelles, qui reconnaissent l'absence du soi. Et l'utérus en regorge. L'embryon échapperait à la destruction car ses enveloppes portent un autre type de protéines HLA, appelées HLA-G, qui agissent comme des immunosuppresseurs.
Quant aux cellules cancéreuses, elles produisent des antigènes anormaux qui devraient également entraîner leur destruction par le système immunitaire. Peut-être y échappent-elles par le mécanisme décrit ci-dessus. Leur furtivité pourrait aussi être liée au fait que ce ne sont pas de bonnes « présentatrices » d'antigènes : elles ne délivreraient pas le second signal adéquat. Autre hypothèse : les cellules cancéreuses libèrent des signaux captés par les cellules immunitaires, les poussant à un suicide anticipé ou rendant leur réponse inefficace. Ces hypothèses ne sont pas exclusives : l'homme évolue avec ses tumeurs depuis des millions d'années, aux cours desquelles a dû s'instaurer un dialogue complexe entre ces dernières et le système immunitaire.
D'où viennent les allergies ?
Ce sont des réactions immunitaires exacerbées - et surtout mal aiguillées. Leur nom fait référence à cette réponse particulière du grec allos , autre, et ergon , travail. La rougeur, l'oedème, les démangeaisons sont dus à la libération dans la peau, dans les muqueuses du nez, dans les bronches, de grandes quantités de substances chimiques responsables de l'inflammation, en particulier de l'histamine. Ces substances font partie intégrante d'une réponse immunitaire normale, mais la machine s'est emballée.
Même si seulement 10 à 20 % des personnes s'en plaignent, tout le monde est plus ou moins allergique. C'est une question d'équilibre dans la réponse immunitaire. Un antigène peut, une fois qu'il a été reconnu par les lymphocytes T auxiliaires, donner lieu à deux réponses différentes. Schématiquement, la première voie recrute les lymphocytes tueurs et permet le rejet des greffes ou la lutte antivirale. La seconde, mise en jeu dans la lutte contre les parasites et beaucoup de bactéries, favorise la formation d'anticorps. Ces voies ont été baptisées TH1 et TH2 pour T helper 1 et 2, parce qu'elles sont mises en route par deux types de lymphocytes auxiliaires, qui émettent des signaux différents. Dans l'allergie, la balance penche vers TH2, et en particulier vers la production d'un type d'anticorps appelé IgE pour immuno- globuline E. Ces anticorps stimulent la libération explosive de l'histamine et d'autres signaux par des cellules spécialisées, les mastocytes.
Certains antigènes - comme ceux des pollens des graminées, qui donnent le rhume des foins - sont plus propices à la production d'IgE. Mais l'allergie est aussi une question de prédisposition génétique : certaines personnes sont plus disposées à répondre par l'une ou l'autre des deux voies immunitaires.
Les éponges, les oiseaux, les végétaux ont-ils un système immunitaire ?
Tout dépend de ce qu'on appelle immunité. Les éponges ou les colonies de coraux sont capables de rejeter un élément étranger. Il s'agit d'un système de reconnaissance du non-soi, mais qui n'a rien à voir avec l'immunité assurée par les lymphocytes. De même, les plantes, les insectes peuvent réagir à un agresseur en relarguant des substances toxiques antibiotiques, protéines. Mais il n'y a pas de reconnaissance précise de l'antigène.
Ce type d'immunité non spécifique, sans mémoire, a bizarrement été qualifiée de « naturelle » ou d'« innée ». Elle correspond, chez l'homme, à l'action des cellules tueuses naturelles, des macrophages ou du complément.
Des molécules, dont la structure est proche de celle des anticorps, ont été retrouvées chez les vers nématodes ou les insectes. Mais cela n'implique pas une parenté de fonction. L'immunité spécifique ou « adaptative » apparaît chez les vertébrés. Presque tous ont un système immunitaire avec des anticorps. A une exception près : on n'en a pas retrouvé chez les vertébrés les plus primitifs, les poissons sans mâchoires ou agnathes, comme la lamproie. Les poissons, les batraciens, les reptiles, les oiseaux ont un thymus. La coopération entre lymphocytes, qui permet la maturation de la réponse immunitaire, atteint son efficacité maximale chez les mammifères.
DOCUMENT larecherche.fr LIEN |